活性氧与线粒体自噬平衡
美国密歇根大学华人学者徐浩新发现的这一现象,是活性氧生物学效应的典型案例,此效应是活性氧激活细胞内处理蛋白废物的溶酶体功能,启动机制是TRPML1离子通道被氧化激活,并继续引起细胞发生自噬,并对细胞氧化应激产生抑制作用,这是一种氧化和控制氧化的平衡调节,也代表活性氧的信号调节作用。研究也提示,细胞不能过于还原,或者过分还原可能会干扰某些关键细胞功能的发挥,氧化还原平衡才能保持细胞健康。
活性氧对细胞的作用有双面性,不仅是产生氧化损伤的基础,也是细胞发挥正常功能的基础。细胞内活性氧水平主要决定于抗氧化系统和活性氧产生的动态平衡,细胞活性氧的主要来源是线粒体代谢副产品。活性氧产生和抗氧化系统之间失去平衡会导致细胞内活性氧水平增加或氧化应激。氧化应激是衰老、多种代谢和神经退行性疾病发生的基础。活性氧过度增加也能引起蛋白质和脂质分子氧化损伤。适度增加活性氧能作为信号能诱发自噬和其他细胞存机制。不健康的线粒体产生活性氧增加,因此活性氧诱导的线粒体自噬对于减少受损线粒体产生活性氧有正面作用,构成细胞内减少氧化损伤的一种负反馈调节机制。
自噬是一种复杂的生物过程,包括启动、自噬体形成、溶酶体产生、自噬体溶酶体融合和降解等过程。活性氧能诱导自噬发生,但过去对这种过程的内在机制并不十分清楚。一种半胱氨酸蛋白酶ATG4是参与细胞自噬的分子,最近被确定是活性氧效应分子。ATG4被氧化可以促进LC3脂化,LC3脂化是细胞自噬启动的关键步骤。考虑到氧化应激往往是一种慢性过程,推测自噬体溶酶体融合可能是氧化应激产生作用的关键过程。
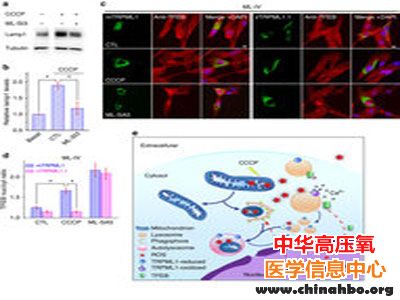
TRPML1是TRP(transient receptorpotential)离子通道蛋白,分布在细胞内体和溶酶体。最近研究发现,TFEB核转位受到溶酶体钙离子的调节,溶酶体钙离子主要是TRPML1调控。但是过去不清楚TRPML1是否影响氧化应激或营养缺乏诱导的细胞自噬过程。溶酶体是控制线粒体质量的关键细胞器,氧化应激是溶酶体功能紊乱疾病的共同特征。线粒体是细胞内活性氧的主要来源,而这些活性氧产生部位和溶酶体非常接近。来自线粒体的活性氧有可能会对溶酶体产生影响。
徐浩新等最新研究发现,这种溶酶体蛋白TRPML1是细胞内氧化应激的感受器,激活后能促进细胞的自体吞噬活性,加速对受损线粒体的清除,从而减少线粒体产生自由基。
钙通道TRPML1作为溶酶体自由基感应器,可以产生强大反馈保护机制抵御自由基带来的损伤。这非常类似于细胞内抗氧化转录因子Nrf2的调节方式,Nrf2是多种抗氧化酶和抗氧化蛋白的关键转录因子,正常情况下在细胞内与Keap1结合,后者在泛素化酶介导下将Nrf2水解。在自由基水平增加时,Nrf2与Keap1分离进入细胞核发挥转录作用。两类抗氧化系统的共同调节方式都是细胞发生氧化应激,或者说活性氧是启动抗氧化的信号分子。这正是自由基反馈调节的模式,非常符合细胞氧化还原平衡的流行观点,并不是少数人说的否定了自由基衰老学说。
正如论文通讯作者徐浩新教授所说,自由基是一把“双刃剑”,既能造成细胞损伤,又能激活保护机制。如果有化学化合物可以激活这个通道,就能降低导致衰老等疾病的氧化应激作用,发挥抗衰老和治疗某些氧化损伤的作用。徐浩新博士本科毕业于北京大学,美国乔治亚州立大学博士学位,2010年荣获美国青年科学家总统奖。近年来徐浩新博士一直致力于TRPML1功能的研究。
本研究发表在《自然通讯》
http://www.nature.com/ncomms/2016/160630/ncomms12109/full/ncomms12109.html#rd
 此主题相关图片如下:1.jpg
此主题相关图片如下:1.jpg